応用問題から学ぶ”身のまわりの物質”⑦~状態変化の問題2~
- atamamonjid
- 2022年7月13日
「テストが迫ってきた。どうしよう?」
「蒸留って何?再結晶との違いがわからない!」
「水とエタノールの混合液を蒸留するとなんでエタノールと水が分かれるの?」
と悩んでいないでしょうか?
中学生にとって蒸留の問題は難しいものです。
「なんのために蒸留するの?」
「蒸留と再結晶の違いがわからない」
「最初の試験管にたまった液体がなんで燃えるの?」
などとなやんでいる中学生は非常に多いです。
そこで今回は、「蒸留の問題を繰り返しといて、蒸留を得意になろう !」とよく出題される問題を実際に解いていきます。
実は、この蒸留の問題は、「また同じ問題が出た」「また同じ実験だった。」というように、ワンパターンであることが多いのです。
特に、同じような図を使っていることが多いので、必然的に同じような問題が出されることになります。
この記事を読み終えたとき、「蒸留の問題はバッチリ」と自信が持てるようになるでしょう。
また、どのような問題が出されるのかを知ってからワークなどを解くことにより「ここが大切!」ということがわかるようになります。効率よく学習することができるのです。
それでは前回に引き続き、私が考えた実践問題をもとに応用力を養っていきましょう。
本記事の特徴
・応用問題(実力テストや高校入試に近い問題)を解くことで、実践力を身に付けることができる
・徐々に難しい問題が解けるようになることで、自信がついていく
それでは、詳しい説明です。
1 まずは基本的な問題を解こう!!(レベル1)
問題1 水20m Lとエタノール5mLの混合液を枝付きフラスコに入れ、下の図のような装置で加熱して沸騰させた。出てきた気体をビーカーで冷やして液体にして、試験管3本に3mLずつ集めた。その後、ガスバーナーの火を消した。試験管A~Cに集まった気体に火をつけると、Aはよく燃えたが、Cになると燃えなかった。次の問いに答えなさい。
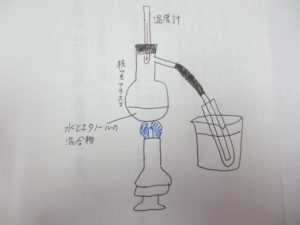
(1)液体が沸騰する温度を何というか。
(2)液体を加熱して沸騰させ、出てくる気体を冷やして再び液体にすることを何というか。
(3)ガスバーナーの火を消す前にしなければならないことは何か。
(4)試験管A~Cに集まった液体について、正しく述べたものをア〜エから1つ選びなさい。
ア 試験管A~Cの液体の中で、エタノールの割合が最も多いのはAの液体である
イ 試験管A~Cの液体の中で、水の割合が最も多いのはAの液体である
ウ 試験管Aの液体は、純粋なエタノールである
エ 試験管Bの液体は、純粋な水である
それでは、レッツ シンキング タイム です。
しっかり考えて、自分なりの答えを持ってから解答と解説を読みましょう。
いかがでしたか?
「難しくてわからなかった!」でしょうか?
そのような人も大丈夫です。
このページを読み終える頃には、「簡単だな」と思えるようになっているでしょう。
それでは、解答と解説です。
【解答】
(1)沸点
(2)蒸留
(3)試験管に集めた液体に、ガラス管の先が入らないようにする
(4) ア
【解説】
(1)液体が沸騰して気体になる時の温度を「沸点」と言います。
沸点は物質によって温度が決まっています。
沸騰と間違えやすい現象が「蒸発」です。
「蒸発」は液体の表面からのみ気体に状態変化する温度で、温度は決まっていません。
この問題とは直接関係ありませんが、「沸騰」と「蒸発」の違いに注意しましょう。
(2)液体の混合物を加熱して沸騰させ、出てきた気体を冷やして再び液体として集める方法を「蒸留」と言います。
間違えやすいのが「再結晶」です。
「蒸留」は液体の混合物を扱うので、「液体」が集まります。
「再結晶」は再び結晶として取り出すので「固体」が取り出せます。
迷ったら
液体として取り出すか、固体として取り出すか
で判断しましょう。
(3)火を消すときにガラス管の先が液体に入っていると、フラスコが冷えた時にその液体を吸い込みます。
加熱した部分に急に冷たい液体が触るとふれるとガラスが割れてしまうので、逆流しないように「火を消す時にはガラス管の先を液体に入れない」ようにします。
(4)間違えやすいのが「ウ」です。
蒸留したと言っても、完全に純粋な物質を集められるわけではありません。
だから、
「エタノールのわりあいが最も高い(エタノールが最も多く含まれている)」
という内容の選択肢を選びましょう。
いかがでしたか?
「まだ難しいよ」という人もいたかもしれません。
そんな人は、ぜひ次の問題を解いてみましょう。
問題2 右の図のように、枝付きフラスコに沸騰石とエタノール3m L、水20m Lを入れて加熱した。出てきた気体をある方法で液体にし、試験管A~Cに2mLずつ集めた。次の問いに答えなさい。
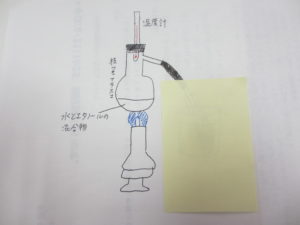
(1)フラスコに沸騰石を入れた理由を説明しなさい。
(2)出たきた気体を液体にするにはどうしたら良いか。図の黄色い四角の部分に実験の方法を図で書きなさい。
(3)試験管Aと試験管Cに集まった液体を比べると性質に違いが見られた。この違いを調べる方法として適したものを下のア〜エから全て選びなさい。
ア 液体のにおいをかぐ
イ 液体に赤色リトマス紙をつける
ウ 液体に赤インクを入れる
エ 液体(液体にひたしたろ紙)に火をつける
オ 液体にフェノールフタレイン液を入れる
どうでしょうか?
それではやってみましょう。!!
解答と解説です。
【解答】
(1)急な沸騰をふせぐため(突沸をふせぐため)
(2)
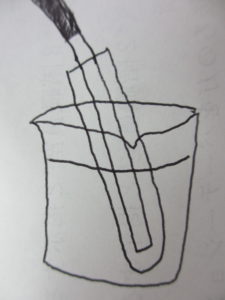
(3)ア エ
【解説】
(1)沸騰石は「急な」沸騰をふせぐために入れます。
よくある間違えが「沸騰をふせぐため」という物です。
沸騰石を入れても沸騰はします。
(2)気体を冷やすと液体になります。
どのように冷やすかと言うと、実験のようにビーカーに入れた水で冷やします。
(3)水とエタノールの混合物を蒸留すると最初にエタノールが多く集まります。
エタノールは独特のにおいと燃えやすい性質があります。
(4)液体の混合物を加熱して沸騰させ、出てきた気体を冷やして再び液体として集める方法を「蒸留」と言います。
「さっき見た問題だ!」と思った人は多いのではないでしょうか?
なぜ同じ問題に見えたかというと、図がほとんど同じだからです。
蒸留の図はなぜかほぼ同じ物が使われます。
そうすると当然、同じような問題が出ます。
だから
最初は難しいけれど、慣れると簡単な問題が増えてくるのです。
では、次の問題を解いて、自信と実力を高めていきましょう。
2 レベルアップをしていこう~「あれ?これって難しい問題?」と思えるかな(レベル2)
問題3 水とエタノールの混合物を加熱する実験を行った。次の問いに答えなさい。
<実験>
①枝付きフラスコに、水20m Lとエタノール3mLを入れ、さらに固体Xを入れた。
②下の図のような装置でゆっくりと加熱した。
③出てきた液体を順に3本の試験管に3m Lずつ集めた。
④試験管A~Cにたまった液体にひたしたろ紙を、それぞれ蒸発皿に入れ、火がつくかどうかを調べた。

(1)液体を加熱して沸騰させ、出てくる気体を冷やして再び液体として集める方法を何というか。
(2)加熱する前にフラスコに入れた固体Xは何か。また、固体Xを入れた理由を説明しなさい。
(3)実験3で、試験管Aにたまった液体のみに火がついた。この理由を「沸点」という言葉を用いて説明しなさい。
それでは考えてみましょう。
レッツ シンキング タイム!!
解答と解説です。
【解答】
(1)蒸留
(2)沸騰石 急な沸騰をふせぐため(突沸をふせぐため)
(3)沸点が低いエタノールが最初に出てきやすいため
【解説】
(1)そろそろ「また蒸留?聞き飽きたよ !」
という人が出てきそうなので、解説しません。
(2)液体を加熱する前には急に沸騰するのを沸騰さするため、沸騰石を入れます。
(3)蒸留は沸点の低い物質から先に出てきます。
ここまで来ると
「また同じ問題?もう飽きたよ!」
という人が増えてきたと思います。
もう一息で蒸留を極めることができます。
もう少しだけがんばりましょう。
本日、最後の問題です。
問題4 下の図のようにして、枝付きフラスコに水30m Lとエタノール3mLの混合物を入れr加熱したところ、やがて気体が出てきた。出てきた気体を水で冷やして液体にし、試験管A~Cに3mLずつ集めた。次の問いに答えなさい。

(1)フラスコに沸騰石を入れたのはなぜか。
(2)水とエタノールの混合物を加熱した時の時間と温度の関係を表したグラフで、最も適当なものをア〜エから1つ選びなさい。
(3)試験管A~Cのなかで、最もエタノールが多く含まれているのはどれか。
(4)(3)のように考えた理由を「沸点」という言葉を用いて説明しなさい。
(5)この実験のように、液体の混合物を加熱して沸騰させ、出てきた気体を冷やして液体として集める方法を何というか。
「あ、簡単!」と思えたのではないでしょうか?
強いていうのであれば、(2)が若干難しかったかもしれません。
それでは解答と解説です。
【解答】
(1)急な沸騰をふせぐため
(2)ウ
(3)試験管A
(4)沸点の低いエタノールが先に出てくるから
(5)蒸留
【解説】
(1)この問題もそろそろ「また出たの?あきたよ!」
と言われそうなので、解説しません。
(2)純粋な物質の融点や沸点は一定ですが、混合物の融点や沸点は一定ではありません。
また、エタノールの沸点を越えると若干緩やかにな流ので、ウになります。
(3)これも、「また同じ問題?」と言われそうなので解説しません。
(4)(3)と同じで「また同じ?」ですよね。
(5)・・・はい・・・またですね・・・解説は・・・いいですね。
以上でした。
「最初はわからなかったけど、わかるようになった」でしょうか?
それでは今日はここまでとします。お疲れさまでした。
